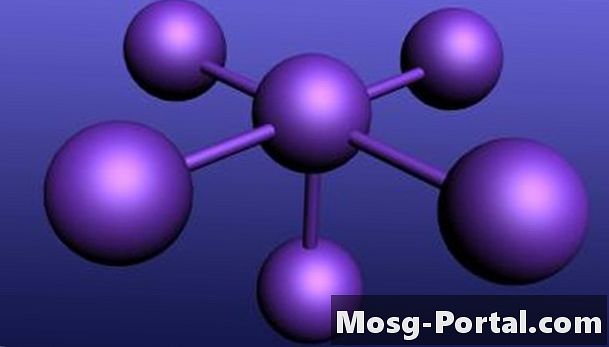
Die molekulare Polarität tritt auf, wenn Atome mit unterschiedlichen Elektronegativitätsraten auf eine Weise kombiniert werden, die zu einer unsymmetrischen Verteilung der elektrischen Ladung führt. Da alle Atome ein gewisses Maß an Elektronegativität aufweisen, sollen alle Moleküle etwas dipol sein. Wenn jedoch ein Molekül eine symmetrische Struktur besitzt, heben sich die Ladungen auf, was zu einem unpolaren Molekül führt. Dasselbe passiert, wenn alle Atome eines Moleküls die gleiche Elektronegativität aufweisen.
Bestimmen Sie die Elektronegativität jedes Atoms mithilfe eines Periodensystems der Elemente. Wenn alle Atome die gleiche Elektronegativität aufweisen, ist das Molekül standardmäßig unpolar. In Anbetracht des Moleküls CH4 hat Kohlenstoff (C) eine Elektronegativität von 2,5 und Wasserstoff (H) eine von 2,1. In Anbetracht des Moleküls NH3 hat Stickstoff (N) eine Elektronegativität von 3,0. Da jedoch das Molekül NCl3, Stickstoff und Chlor die gleiche Elektronegativität von 3,0 aufweisen, ist das Molekül unpolar.
Zeichnen Sie das Molekül mit der Lewis-Punktdiagramm-Methode. Zählen Sie die Anzahl der Valenzelektronen, die jedes Atom enthält. Ordnen Sie die Atome so an, dass sich das Atom mit der größten Elektronegativität im Zentrum befindet. Verbinden Sie die Atome mit Einfachelektronenbindungen und entfernen Sie diese Elektronen aus der Valenzzählung. Positionieren Sie Elektronenpaare um die äußeren Atome, bis Sie ein Oktett erhalten, und entfernen Sie diese Elektronen aus der Zählung. Platziere alle verbleibenden Elektronen um das Atom in der Mitte.
Bestimmen Sie die Polarität der Moleküle, indem Sie deren Form auf Symmetrie untersuchen. In diesem Beispiel hat das Molekül CH4 eine tetraedrische Form, die symmetrisch ist. Somit ist es unpolar. Das Molekül NCl3 hat andererseits eine Pyramidenform, ist also polar. Im Allgemeinen sind Moleküle mit linearen, trigonalen und tetraedrischen Formen unpolar, während Atome mit pyramidenförmigen und V-förmigen Formen polar sind.