Inhalt
Wenn Sie die formale Ladung eines Moleküls wie CoCl2 (Phosgengas) bestimmen, müssen Sie die Anzahl der Valenzelektronen für jedes Atom und die Lewis-Struktur des Moleküls kennen.
Valenzelektronenzahl
Schlagen Sie jedes Atom im Periodensystem der Elemente nach, um die Anzahl der Valenzelektronen zu bestimmen.
Denken Sie daran, dass zwei Elektronen in die erste s-Schale, zwei Elektronen in die zweite s-Schale, sechs Elektronen in die erste p-Schale usw. gehen. Zur Erinnerung: 1s (^ 2) 2s (^ 2) 2p (^ 6) 3s ( ^ 2) 3p (^ 6)
Zum Laden anpassen. Wenn das Molekül ein Ion ist, addieren oder subtrahieren Sie insgesamt ein oder mehrere Elektronen, um die endgültige Ladung zu erklären.
Für CoCl 2 (Phosgengas): C = 4; O = 6; Cl = 7. Das Molekül ist nicht ionisiert und neutral geladen. Daher beträgt die Gesamtmenge der Valenzelektronen 4 + 6 + (7x2) = 24.
Lewis-Struktur
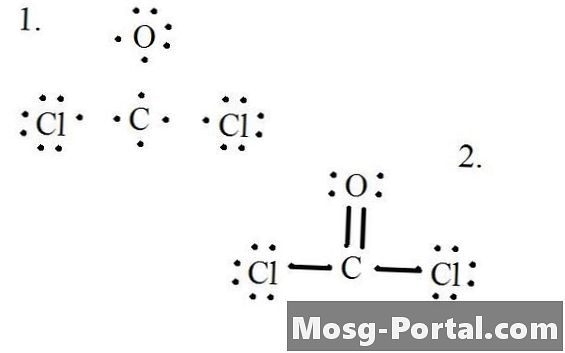
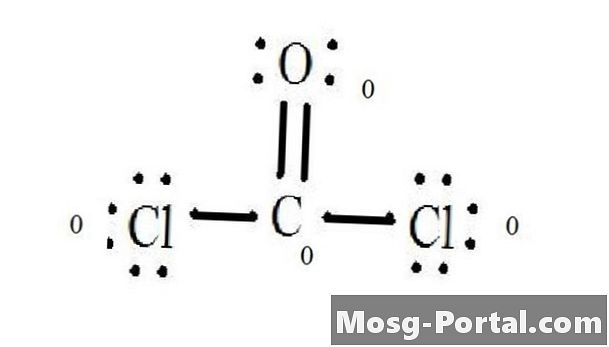
Siehe das Diagramm für die Lewis-Struktur von CoCl2 (Phosgengas). Die Lewis-Struktur repräsentiert die stabilste und wahrscheinlichste Struktur für ein Molekül. Atome werden mit gepaarten Valenzelektronen gezeichnet; Zwischen einzelnen Elektronen werden Bindungen gebildet, um die Oktettregel zu erfüllen.